三阴性乳腺癌(triple-negative breast cancer,TNBC)恶性程度高、转移能力强,由于不表达雌激素受体、孕激素受体和人表皮生长因子受体-2,缺乏明确的靶标,其药物治疗方式主要为化疗,然而效果并不理想。
TNBC与其他乳腺癌亚型不同,其代谢表型主要为线粒体代谢,抑制线粒体代谢是治疗TNBC的潜在途径。由于正常细胞也存在线粒体,应用直接靶向线粒的药物存在风险,亟需寻找调控TNBC线粒体功能和活性的关键信号及药物干预策略。
近日,我校天然药物资源优效利用重点实验室陈妍/沈祥春团队在国际知名期刊《Journal of Experimental &Clinical Cancer Research》(IF: 11.4,中科院医学1区,TOP期刊)上在线发表研究论文“Shikonin blocks CAF-induced TNBC metastasis by suppressing mitochondrial biogenesis through GSK-3β/NEDD4-1 mediated phosphorylation-dependent degradation of PGC-1α”。该研究从肿瘤细胞与微环境互作的角度,揭示了TNBC细胞在转移过程中线粒体生物合成上调的机制,并发现天然产物紫草素能够通过阻断TNBC细胞线粒体生物合成发挥治疗效应。

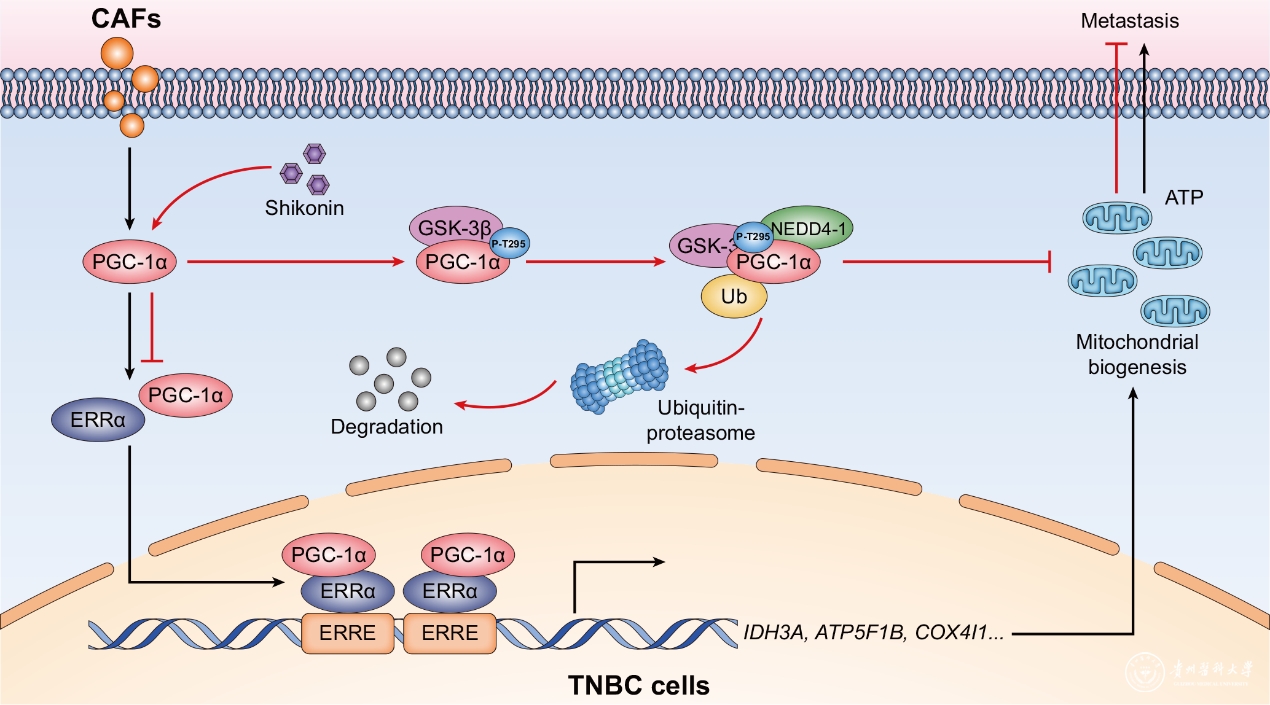
该项研究显示,肿瘤相关成纤维细胞通过上调TNBC细胞中过氧化物酶体增殖物激活受体γ辅激活因子1α(PGC-1α)的表达和活性,激活PGC-1α/ERRα信号轴促进TNBC细胞线粒体生物合成。天然产物紫草素通过GSK-β上调PGC-1α蛋白295位酪氨酸的磷酸化,增强泛素连接酶NEDD4-1对PGC-1α蛋白中“TPPTTPP”序列的识别,介导了PGC-1α的泛素化降解,下调PGC-1α的表达,从而抑制肿瘤相关成纤维细胞诱导TNBC细胞线粒体生物合成,发挥抗TNBC转移的活性。
该研究由陈妍/沈祥春教授团队以及暨南大学齐琦教授团队共同完成。博士研究生樊双琴为论文第一作者、硕士研究生宴小敏以及胡晓霞副教授为论文共同第一作者,陈妍、齐琦、沈祥春为论文通讯作者。该研究得到了国家自然科学基金(82273957和81973341)、贵州省创新平台建设项目([2023]003)、贵州省自然科学基金(QKHJC-ZK(2021)-YB562和QKHJC-ZK(2023)ZD-034),贵州省优秀青年科技人才计划(QKHPTRC(2021)-5632)以及米兰milan(中国)优秀青年人才计划([2020]101)等基金资助。
原文链接:https://jeccr.biomedcentral.com/articles/10.1186/s13046-024-03101-z
 公网安备 52010302000012号
公网安备 52010302000012号